 Điện thoại
Điện thoại
 Laptop
Laptop
 Phụ kiện
Phụ kiện
Sạc dự phòng
Sạc, cáp
Ốp lưng điện thoại
Ốp lưng máy tính bảng
Miếng dán
Miếng dán Camera
Túi đựng AirPods
Quạt mini
HotBút tablet
Giá đỡ điện thoại/laptop/máy tính bảng
Dây đeo điện thoại
Ống kinh điện thoại
MớiHub, cáp chuyển đổi
Chuột máy tính
Bàn phím
Router - Thiết bị mạng
Balo, túi chống sốc
Túi đựng phụ kiện
Phủ phím laptop
Phần mềm
Giá treo màn hình
Đèn thông minh/livestream
MớiMiếng lót chuột
Bảng vẽ điện tử
MớiTai nghe Bluetooth
Tai nghe dây
Tai nghe chụp tai
Tai nghe thể thao
Loa
HotMicro
Kính thông minh
MớiCamera Giám Sát
HotCamera trong nhà
Camera ngoài trời
Camera hành trình / hành động
HotCamera Năng Lượng Mặt Trời
Camera 4G
 Smartwatch
Smartwatch
 Đồng hồ
Đồng hồ
 Tablet
Tablet
 Máy cũ, Thu cũ
Máy cũ, Thu cũ
Máy cũ giá tốt
Thu cũ đổi mới
 Màn hình, Máy in
Màn hình, Máy in
 Sim, Thẻ cào
Sim, Thẻ cào
 Dịch vụ tiện ích
Dịch vụ tiện ích
Đóng tiền trả góp
Đóng tiền điện
Đóng tiền nước
Đóng tiền NET FPT
Đóng tiền net, cáp VNPT
Thu vé tàu, xe, máy bay
Bảo hiểm xe máy - Ô tô
Đóng BHYT- BHXH
Vay tiền mặt CAKE
Vay tiền mặt CATHAY
Bảo hành rơi vỡ
Bảo hành mở rộng
Bảo hành 1 đổi 1
Mua gói data 3G, 4G
Nạp tiền trả trước
Nạp tiền trả sau
Thẻ cào game
Thẻ cào điện thoại
Đặt vé máy bay
Nạp rút tài khoản ngân hàng

Không tìm thấy kết quả phù hợp
Hãy thử lại với từ khoá khácHãy chọn địa chỉ cụ thể để chúng tôi cung cấp chính xác giá và khuyến mãi

Hiệu suất là gì?
Hiệu suất là khả năng để làm một việc gì đó hay tạo ra kết quả mong muốn bằng lượng một cách tối đa bằng nguồn lực cố định. Hiệu suất phản ứng trong hóa học là lượng sản phẩm tối đa (sản phẩm thực tế) mà một phản ứng hoá học có thể tạo ra.

Công thức tính hiệu suất

Ví dụ bài toán tính hiệu suất
Khối lượng chất tham gia phản ứng sẽ lớn hơn lượng chất được tính toán, để bù vào lượng chất đã bị hao hụt trong quá trình phản ứng, do hiệu suất phản ứng phải luôn nhỏ hơn 100%.

Công thức khối lượng chất
Lượng sản phẩm thực tế của một phản ứng khi đã xác định được khối lượng tham gia phản ứng, kèm theo đó là hiệu suất phản ứng nhỏ hơn 100% nên khối lượng sản phẩm tạo ra sẽ bị hao hụt đi một phần. Công thức tính được khối lượng sản phẩm thực thế là:

Công thức khối lượng chất
Đề bài: Nung nóng 1,2 mol CaCO3 thì ta thu được 0,96 mol CaO. Hãy tính hiệu suất phản ứng hóa học xảy ra.
Phương trình phản ứng: CaCo3 → Cao + CO2
Theo lý thuyết thì phản ứng trên ta có 1,2 mol CaCO3 tạo 1,2 mol CaO.
Kết quả thực tế thì chỉ đo được 0,96 mol CaO.
→ CaO lượng tính toán theo phản ứng là 1,2 (gọi là khối lượng theo lý thuyết) và lượng chắc chắn thu được là 0,96 (gọi là lượng thực tế).
→ Hiệu suất phản ứng
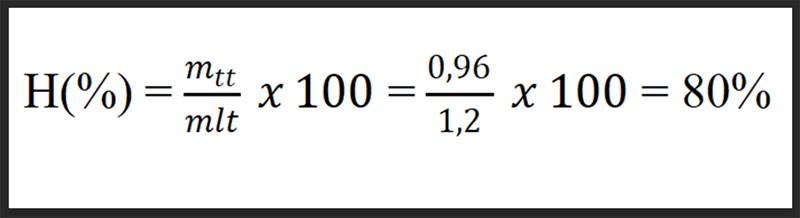
Tính hiệu suất phản ứng
Xem thêm:
Hy vọng bài viết về hiệu suất này có thể giúp bạn có thêm được kiến thức trong quá trình giải những bài tập hóa thú vị. Hãy chia sẻ bài viết đến bạn bè để cùng hiểu hơn nhé!
↑
ĐĂNG NHẬP
Hãy đăng nhập để Chia sẻ bài viết, bình luận, theo dõi các hồ sơ cá nhân và sử dụng dịch vụ nâng cao khác trên trang Game App của
Thế Giới Di Động
Tất cả thông tin người dùng được bảo mật theo quy định của pháp luật Việt Nam. Khi bạn đăng nhập, bạn đồng ý với Các điều khoản sử dụng và Thoả thuận về cung cấp và sử dụng Mạng Xã Hội.